rhGM-CSF, гранулоцитарно-макрофагальный колониестимулирующий фактор человека, рекомбинантный белок
Синонимы: Granulocyte-macrophage colony stimulating factor, GM-CSF, Colony stimulating factor 2, CSF2.
Источник: Клеточная линия CHO, продуцирующая rhGM-CSF.
Чистота: >97% в соответствии с электрофорезом в ПААГ с последующим окрашиванием Coomassie Brilliant Blue.
Уровень эндотоксина: <1.0 EU на 1 мкг белка, LAL-тест.
Молекулярный вес: Вследствие посттрансляционных модификаций и гликозилирования белок rhGM-CSF мигрирует широкой полосой на уровне между 25 и 35 кДа в ПААГ.
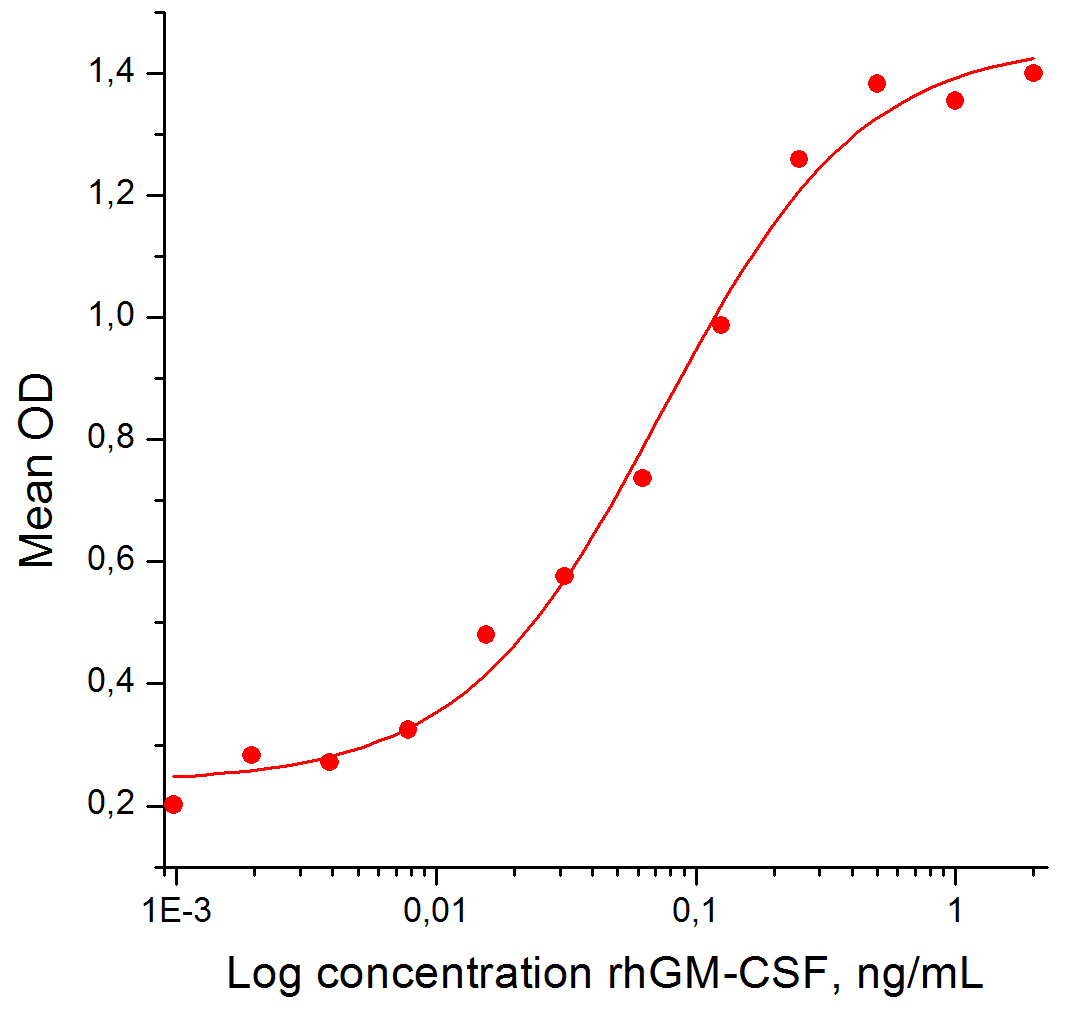
Биологическая активность: Рекомбинантный белок rhGM-CSF человека стимулирует пролиферацию клеток линии эритролейкоза человека (TF-1). ED50 рекомбинантного белка rhGM-CSF для данного эффекта обычно 0,1-0,6 нг/мл. Оптимальная концентрация для индивидуального применения определятся пользователем.
Форма
Лиофильно высушен из фосфатного буферного раствора PBS, содержащего 0,05% Tween20, pH 7.0, профильтрованного через фильтр с диаметром пор 0,22мкм.
Не содержит вспомогательных белков.
Разведение
Центрифугировать флакон при 1000g, 3 мин. Добавить стерильный фосфатный буферный раствор (PBS) до конечной концентрации 0,1-1 мкг/мкл. Оставить на 20-30 мин при комнатной температуре, затем центрифугировать при 1000g в течение 1 мин, и мягко ресуспендировать. Для приготовления рабочих растворов можно использовать буфер на водной основе или культуральную среду. Добавление вспомогательных белков (BSA или FBS) не является необходимым.
Условия транспортировки
Перевозить при комнатной температуре.
Стабильность и Условия хранения:
- 24 месяца, хранение невскрытой упаковки, при температуре от -20 до -70°C.
- 1 месяц, разведенный в стерильных условиях, при температуре от 2 до 8°C.
- 6 месяцев, разведенный в стерильных условиях, при температуре от -20 до -70°C.
Не рекомендуются повторные циклы замораживания-оттаивания раствора рекомбинантного белка.
rhGM-CSF (# PSG030) был использован в следующих работах:
Glycan recognition by human blood mononuclear cells with an emphasis on dendritic cells
Eugenia M. Rapoport, Sergey V. Khaidukov, Andrey M. Gaponov, Galina V. Pazynina, Svetlana V. Tsygankova, Ivan M. Ryzhov, Ivan M. Belyanchikov, Panagiota Milona, Nicolai V. Bovin, Kenneth C. McCullough.
Glycoconjugate Journal volume 35, pages191–203(2018) https://doi.org/10.1007/s10719-017-9811-6
Dilyara Nurkhametova, Andrei Siniavin3, Maria Streltsova, Denis Kudryavtsev, Igor Kudryavtsev, Raisa Giniatullina, Victor Tsetlin, Tarja Malm and Rashid Giniatullin
Front. Cell. Neurosci., 28 October 2020 | https://doi.org/10.3389/fncel.2020.548376
| Описание | |
| Дополнительное описание и цитирование |
Гранулоцитарно-макрофагальный колониестимулирующий фактор, (GM-CSF, от англ. Granulocyte Macrophage Colony-Stimulating Factor), является гемопоэтическим ростовым фактором и модулятором иммунного ответа. GM-CSF человека представляет собой мономерный белок из 127 аминокислот с двумя сайтами гликозилирования. Вариабельность гликозилирования приводит к различиям в молекулярной массе в интервале от 14 кДа до 35 кДа. Негликозилированный и гликозилированный GM-CSF демонстрирует сходную активность in vitro. Рецептор GM-CSF (GM-CSFR) – это гетеродимер образованный α субъединицей (GM-CSFRα или CD116; 60-80 kDa) и β субъединицей (GM-CSFRβс или CD131; 120-140 kDa), которая представляет собой часть комплекса рецепторов IL-3 и IL-5. GM-CSF поддерживает жизнеспособность, пролиферацию и дифференцировку по пути акитвации Янус-киназы 2 (JAK2) с последующим фосфорилированием сигнального белка-трансдуктора и активатора транскрипции STAT5 (pSTAT5). Наличие широкого пула клеток, экспрессирующих поверхностный рецептор GM-CSFR, подтверждает многофункциональную активность GM-CSF. Выявлено, что GM-CSF активирует и поддерживает Тh1 зависимый иммунный ответ, ангиогенез, развитие аутоиммунных заболеваний и аллергического воспаления. В клинической практике GM-CSF применяется с целью уменьшения выраженности нейтропении (после противоопухолевой химиотерапии) и лейкопении (в случаях недостаточности костномозгового кроветворения), инфекционных заболеваний (включая ВИЧ-инфекцию), после аутологичной или сингенной трансплантации костного мозга. GM-CSF имеет широкий диапазон лимфоидной регуляторной активности, связывая врожденный и адаптивный иммунитет, являясь триггером гемопоэтических и лимфоидных факторов, и в этой связи является ключевым адъювантом в разработке подходов к лечению всех видов заболеваний требующих компетентного иммунного ответа. Использованная литература:
|