Стабильность рекомбинантных белков - это не миф
Умеренный скептицизм присущ всем ученым-исследователям. Практика подвергать сомнению достоверность концепций, у которых отсутствуют экспериментальные доказательства и воспроизводимость результатов — является частью объективного научного исследования. Поэтому, прежде чем опубликовать свои данные (описание продукта,фотографии гелей, графики), мы подвергаем их многократной проверке и здесь приводим часть наших результатов.
Термин «стабильность» белковых молекул в классической биохимии используется при рассмотрении пространственной структурной организации белковой глобулы и характеристики ее термодинамического состояния. Мерой стабильности белка является свободная энергия, которая определяется его энтальпией, то есть энергией взаимодействия атомов белка, и его энтропией, являющейся мерой числа конформаций, которыми данное состояние белка может быть реализовано. Более стабильному состоянию системы отвечает то, где ниже свободная энергия, а самому стабильному состоянию системы (при заданной температуре и фиксированном объеме этой системы) отвечает минимум свободной энергии. Сворачивание белка заключается в поиске уникальной нативной структуры, отвечающей минимуму свободной энергии, среди большого числа конформаций (Финкельштейн А.В., Птицын О.Б., 2012, Кузнецова И.М., 2005). После сворачивания в высокоорганизованное нативное состояние белок становиться функционально активным. В природе достижение такого состояния обеспечивается за счёт реализации большого ряда сложных биохимических реакций, осуществляемых в процессе биосинтеза белка в живых клетках. Можно говорить о том, что в большинстве случаев нативная конформация белка является необходимым условием стабильности белковой глобулы.
Для обеспечения стабильности полноразмерных рекомбинантных белков, производимых ООО «СайСторЛаб», была разработана собственная оригинальная технологическая платформа, которая в качестве экспрессионной системы использует клеточную линию млекопитающих – CHO (Chinesehamsterovary - клетки яичников китайских хомячков). Экспрессия белков человека именно в клетках млекопитающих, обеспечивает правильный процессинг, фолдинг и корректные посттрансляционные модификации за счёт близкого сходства белоксинтезирующих аппаратов человека и клеток CHO, что гарантирует высокую специфическую активность и стабильность продуцируемых белков.
Анализ биологической активности как показатель стабильности рекомбинантных белков ООО "СайСторЛаб"
При получении и использовании рекомбинантных белков в научно-исследовательской работе и биотехнологическом производстве, термин - «стабильность» используется скорее, как характеристика устойчивости белков к различным денатурирующим воздействиям с сохранением своей специфической функциональной или биологической активности. Срок годности белков, то есть срок сохранения их специфической биологической активности без существенного падения, как раз и определяется стабильностью. Высокий уровень стабильности рекомбинантных белков является крайне желательным, так как допускает возможность их длительного хранения. Немаловажным фактором использования рекомбинантных белков в исследовательских и прикладных целях является экономическая составляющая. Высокая стабильность белка создаёт возможность длительного хранения и, с одной стороны, позволяет приобретать фасовку большего объёма с низкой удельной ценой, а с другой, позволяет экономить время на регулярных манипуляциях по приготовлению сред и исследуемых образцов, так как большие объёмы растворов прекрасно хранятся в холодильнике. Хорошо известно, что среды, приготовленные с содержанием рекомбинантных факторов роста бактериального происхождения (экспрессированными, например, в E.coli) хранятся не более 1 мес. при +4°С, после чего добавки теряют свою биологическую активность. Собственное knowhow ООО «СайСторЛаб» позволяет получать высокостабильные белки, сохраняющие свою биологическую активность в растворах культуральных сред более 12 месяцев. Более того, лиофилизированная форма наших белков, обеспечивает их сохранность без потери активности в случае хранения при комнатной температуре до 30 дней. Таким образом, достигается возможность транспортировки в любые уголки страны без соблюдения холодовой цепи.
Хранение восстановленной (разведённой из лиофилизированной) формы рекомбинантных белков ООО «СайСторЛаб» при температурном режиме от 2 до 8°С в течение 365 дней не приводит к снижению уровня их биологической активности.
В данной публикации на примере рекомбинантного гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ) человека рассматривается возможность длительного хранения без потери стабильности раствора белка, полученного после разведения из аликвоты лиофильно-высушенного рекомбинантного ГМ-КСФ.
ГМ-КСФ был восстановлен используя стерильную воду (MilliQ), до конечной концентрации белка – 1мг/мл. Для определения биологической активности рекомбинантного ГМ-КСФ человека использовали общепринятый и широко используемый тест количественного определения пролиферативной активности фактор-зависимых клеток линии эритролейкоза человека (TF-1). Биологическую активность рекомбинантного ГМ-КСФ человека оценивали путем определения его эффективной дозы (ЭД50), с использованием реагента CellTiter 96®AQueousOneSolutionCellProliferationAssay.
Известно, что живые клетки восстанавливают входящее в состав реагента химическое соединение MTS [3-(4,5-диметилтиазол-2-ил)-5-(3-карбоксиметоксифенил)-2-(4-сульфофенил)-2H-тетразолий, внутренняя соль] с образованием окрашенного продукта восстановления – формазана, который растворяется в среде для культивирования клеток и окрашивает её. Оптическую плотность раствора (среды), содержащей растворенный формазан, измеряли при длине волны 490 нм и 620нм (для исключения влияния фоновыхзначений). Количество восстановленного формазана прямо пропорционально количеству живых клеток в образце.
Эффективную дозу исследуемого раствора ГМ-КСФ определяли по характерной S-образной кривой, построенной в координатах оптическая плотность – массовая концентрация ГМ-КСФ (нг/мл). Для вычисления ЭД50 использовали линейную область кривой, по которой определяли значение массовой концентрации ГМ-КСФ, соответствующей 50% максимально достигнутого биологического эффекта.
Тест на биологическую активность – это мера пролиферативной активности клеток на исследуемый белок. Различные вариации постановки биологического теста, такие как, плотность клеток, число пассажей, культуральная среда и вносимые добавки приводят к вариабельности формы кривой при повторах исследования в разные временные интервалы. К сожалению, в настоящее время невозможно добиться абсолютной идентичности всех условий биологического теста при повторах в разные временные точки. Поэтому при анализе активности цитокинов традиционно используется значение ЭД50.
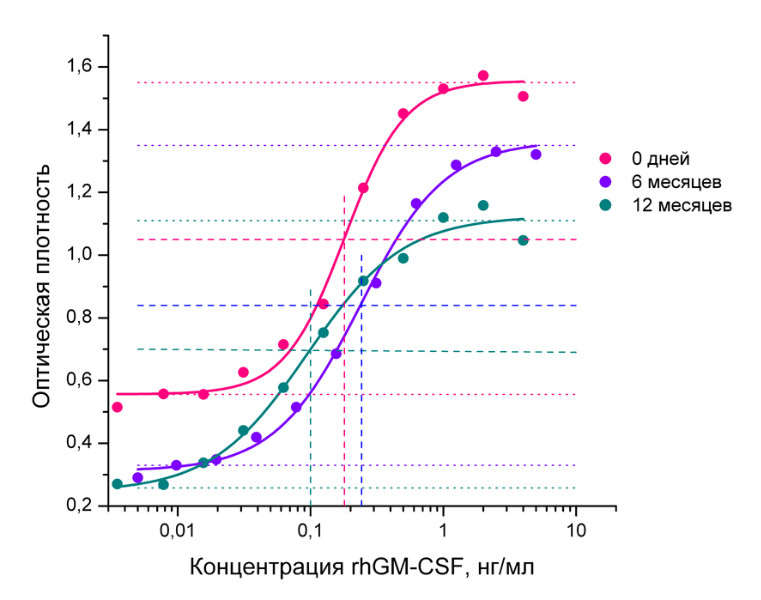
Диапазон значений ЭД50, приведённый для рекомбинантного ГМ-КСФ человека, на рисунке определён с использованием стандартного общепринятого алгоритма. Для каждой экспериментальной S-образной кривой проведены аппроксимирующие линии, определяющие 100% эффекта и 0% эффекта. Середина отрезка, соединяющего пересечение данных прямых с осью ординат (ОП), соответствует эффекту 50%. Концентрация белка, вызывающая 50 % эффект(ответ биологической системы), определяется значением концентрации белка, отложенной по оси абсцисс, и будет являться ЭД50 для данного образца белка (Рисунок 1).
Рисунок 1. Кривые доза-эффект, построенные, на основе анализа пролиферативной активности клеток TF-1 в ответ на добавление ГМ-КСФ, хранившегося в растворе при 2 до 8 °С разные периоды времени.
В ходе тестирования стабильности восстановленного рекомбинантного ГМ-КСФ человека производства ООО «СайСторЛаб» раствор белка хранили при температурном режиме от 2 до 8 °С в течение 12 месяцев. Анализ специфической биологической активности проводили сразу после восстановления, через 6 и 12 месяцев. Кривые, полученные по результатам тестирования пролиферативного ответа клеток TF-1, на разных сроках исследования приведены на рисунке 1. Значения ЭД50, рассчитанные по соответствующим кривым приведены в таблице 1. Полученные значения ЭД50 имеют незначительный разброс и лежат в диапазоне значений, приводимом в спецификации к каждому лоту данного белка.
| Длительность хранения | Значение ЭД50, нг/мл |
|---|---|
| 0 месяцев | 0,18 |
| 6 месяцев | 0,24 |
| 12 месяцев | 0,10 |
Таблица 1. Значения ЭД50 для рекомбианантного ГМ-КСФчеловека производства ООО «СайСторЛаб» на разных сроках хранения в растворе.
Таким образом, длительное хранение восстановленной (растворенной) формы рекомбинантного ГМ-КСФ человека производства ООО «СайСторЛаб» не приводит к снижению его биологической активности.